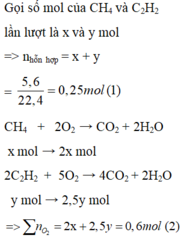Đốt cháy 28ml hỗn hợp khí metan và axetilen cần phải dùng 33.6 ml khí Oxi .Tính % về thể tích của mỗi khí trong hỗn hợp (đktc)

Những câu hỏi liên quan
4.Đốt cháy 28ml hỗn hợp khí metan và axetilen cần phải dùng 67,2ml khí oxi
a) tính phần trăm thể tích của mỗi khí trong hỗn hợp
b) tính thể tích khí CO2 sinh ra
(các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất)
Gọi thể tích metan (CH4) là x (ml); thể tích axetilen (C2H2) là y (ml)
Theo bài ra: Vhh khí = 28 (ml)
→ x + y = 28 (1)
Phương trình phản ứng:
CH4+2O2-to>CO2+2H2O
x--------2x--------------x
2C2H2+5O2-to>4CO2+2H2O
y-----------2,5y---------2y
Theo bài ra thể tích khí oxi là 67,2 ml
→ 2x + 2,5y = 67,2 ml (2)
Từ (1) và (2) giải hệ phương trình được: x = 5,6 (ml) và y = 22,4 (ml).
a/ Phần trăm thể tích từng khí là:
%VCH4=20%
->%VC2H2=80%
b/ Theo phương trình phản ứng ở trên có:
Thể tích khí CO2 = x + 2y = 5,6 + 2.22,4 = 50,4 (ml).
Đúng 1
Bình luận (0)
Đốt cháy 28 ml hỗn hợp khí metan và axetilen cần phải dùng 67.2 ml khí O2 .Tính thể tích mỗi khí trong hỗn hợp đó
\(V_{CH_4} = a(ml) ; V_{C_2H_2} = b(ml)\\ \Rightarrow a + b = 28(1)\\ CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ 2C_2H_2 + 5O_2 \xrightarrow{t^o} 4CO_2 + 2H_2O\\ V_{O_2} = 2a + \dfrac{5}{2}b = 67,2(2)\\ (1)(2) \Rightarrow a = 5,6 ; b = 22,4\\ V_{CH_4} = 5,6(ml) ; V_{C_2H_2} = 22,4(ml)\)
Đúng 1
Bình luận (0)
cho 5,6l(đktc) hỗn hợp khí X gồm metan và etilen qua dd brom dư , khối lượng brom đã tham gia phản ứng là 8g
a) hãy viết pthh
b) tính % thể tích mỗi khí trog hỗn hợp X
c) nếu đốt cháy 28ml hỗn hợp khí X ở trên thì cần dùng bao nhiêu ml khí oxi
C2H4+Br2->C2H4Br2
0,05----0,05
n Br2=\(\dfrac{8}{160}\)=0,05 mol
=>%VC2H4=\(\dfrac{0,05.22,4}{5,6}.100=20\%\)
=>%VCH4=80%
c)CH4+2O2-to>CO2+2H2O
1.10-3----2.10-3 mol
C2H4+3O2-to>2CO2+2H2O
2,5.10-4-7,5.10-4 mol
n hh=\(\dfrac{0,028}{22,4}\)=1,25.10-3 mol
=>n C2H4=2,5.10-4 mol
=>n CH4=1.10-3 mol
=>VO2=(2.10-3+7,5.10-4).22,4=0,0616l
Đúng 3
Bình luận (0)
\(n_{Br_2}=\dfrac{8}{160}=0,05mol\)
\(\Rightarrow n_{etilen}=n_{Br_2}=0,05mol\)
\(n_{hh}=\dfrac{5,6}{22,4}=0,25mol\)
\(\Rightarrow n_{metan}=n_{hh}-n_{etilen}=0,25-0,05=0,2mol\)
a)\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b)\(\%V_{metan}=\dfrac{0,2}{0,25}\cdot100\%=80\%\)
\(\%V_{etilen}=100\%-80\%=20\%\)
Đúng 1
Bình luận (3)
Đốt cháy 28 ml hỗn hợp khí metan và axetilen cần phải dùng 67,2 ml khí oxi.
a) Tính phần trăm thể tích của mỗi khí trong hỗn hợp.
b) Tính thể tích khí CO2 sinh ra.
(Các thể tích khí đo ở cùng điểu kiện nhiệt độ và áp suất).
Bài 4. Đốt cháy 28 ml hỗn hợp khí metan và axetilen cần phải dùng 67,2 ml khí oxi.
a) Tính phần trăm thể tích của mỗi khí trong hỗn hợp.
b) Tính thể tích khí CO2 sinh ra.
(Các thể tích khí đo ở cùng điểu kiện nhiệt độ và áp suất).
Lời giải:
Đối với chất khí, trong cùng điều kiện về nhiệt độ và áp suất, tỉ lệ số mol trong phương trình phản ứng cũng là tỉ lệ về thể tích các khí.
a) Gọi thế tích của CH4 và C2H2 lần lượt là x, у (ml).
Phương trình phản ứng: CH4 + 2O2 → CO2 + 2H2O
p.ư: x -> 2x x (ml)
2C2H2 + 5O2 → 4CO2 + 2H2O
p.ư: у -> 2,5y 2y (ml)
Theo thể tích hỗn hợp và thể tích oxi, ta có hệ phương trình:
Giải (1) và (2), ta được x = 5,6ml và y = 22,4ml.
% =
x 100% = 20%; %
= 100% - 20% = 80%
b) Thể tích khí khí C02 sinh ra = x + 2y = 5,6 + 2 x 22,4 = 50,4ml.
Đúng 0
Bình luận (0)
Dẫn 13.44l (đktc) gồm hỗn hợp metan và axetilen đi qua dd Br dư thì thấy thoát ra 6, 72 lít một chất khí a) tính phần trăm của mỗi khí trong hỗn hợp ban đầu b) tính thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn hỗn hợp khí trên
a.\(n_{hh}=\dfrac{13,44}{22,4}=0,6mol\)
\(n_{C_2H_2Br_4}=\dfrac{6,72}{22,4}=0,3mol\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
0,3 0,3 ( mol )
\(\%C_2H_2=\dfrac{0,3}{0,6}.100=50\%\)
\(\%CH_4=100\%-50\%=50\%\)
b.
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
0,3 0,6 ( mol )
\(2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\)
0,3 0,75 ( mol )
\(V_{O_2}=\left(0,6+0,75\right).22,4=1,35.22,4=30,24l\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 5,6 lít hỗn hợp khí metan và axetilen cần dùng 13,44 lít khí oxi. Phần trăm thể tích mỗi khí trong hỗn hợp là A.
C
H
4
40% và
C
2
H
2
60%. B.
C
H
4
80% và
C
2
H
2
20%. C.
C
H...
Đọc tiếp
Đốt cháy hoàn toàn 5,6 lít hỗn hợp khí metan và axetilen cần dùng 13,44 lít khí oxi. Phần trăm thể tích mỗi khí trong hỗn hợp là
A. C H 4 40% và C 2 H 2 60%.
B. C H 4 80% và C 2 H 2 20%.
C. C H 4 20% và C 2 H 2 80%.
D. C H 4 60% và C 2 H 2 40%.
Đốt cháy 280ml hỗn hợp khí metan và axetilen cần phải dùng 672ml khí oxi.
a) Tính phần trăm thể tích của mỗi khí trong hỗn hợp.
Cứu tui mn ơi
a, \(n_{CH_4}+n_{C_2H_2}=\dfrac{0,28}{22,4}=0,0125\left(mol\right)\left(1\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,0025\left(mol\right)\\n_{C_2H_2}=0,01\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,0025.22,4}{0,28}.100\%=20\%\\\%V_{C_2H_2}=80\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Đốt cháy 4,48 l hỗn hợp khí metan và etilen cần phải dùng 11,2 l khí oxi.
a. Viết các phương trình hóa học của phản ứng.
b. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp.
(Biết rằng thể tích khí đo ở đktc)
a) PTHH: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
b) Đặt \(n_{CH_4}=x\left(mol\right);n_{C_2H_4}=y\left(mol\right)\). Khi đó \(22,4x+22,4y=4,48\) \(\Leftrightarrow x+y=0,2\)
Từ PTHH \(\Rightarrow n_{O_2\left(1\right)}=2x\left(mol\right)\)\(;n_{O_2\left(2\right)}=3y\left(mol\right)\). Khi đó \(2x.22,4+3y.22,4=11,2\) \(\Leftrightarrow2x+3y=0,5\)
Vậy ta có \(\left\{{}\begin{matrix}x+y=0,2\\2x+3y=0,5\end{matrix}\right.\Leftrightarrow x=y=0,1\left(mol\right)\)
\(\Rightarrow\%V_{CH_4}=\%V_{C_2H_4}=50\%\)
Đúng 2
Bình luận (0)
Câu 6Đốt cháy hoàn toàn 6,72lít hỗn hợp khí gồm metan và axetilen, thu được 7,84 lít khí CO2 ở đktc. a. Tính phần trăm theo thể tích của mỗi khí trong hỗn hợp A :b. Tính khối lượng của oxi cần để đốt cháy hoàn toàn hỗn hợp khí trên.
Đọc tiếp
Câu 6
Đốt cháy hoàn toàn 6,72lít hỗn hợp khí gồm metan và axetilen, thu được 7,84 lít khí CO2 ở đktc.
a. Tính phần trăm theo thể tích của mỗi khí trong hỗn hợp A :
b. Tính khối lượng của oxi cần để đốt cháy hoàn toàn hỗn hợp khí trên.
a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\left(1\right)\)
\(n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,25\left(mol\right)\\n_{C_2H_2}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,25.22,4}{6,72}.100\%\approx83,33\%\\\%V_{C_2H_2}\approx16,67\%\end{matrix}\right.\)
Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=0,625\left(mol\right)\Rightarrow m_{O_2}=0,625.32=20\left(g\right)\)
Đúng 3
Bình luận (1)